Cycle du carbone
Type de ressources
Type de ressource multimédia
Contributeur(s)
Thème(s) Scientifique(s) 1er degré
Thème(s) Scientifique(s) 2nd degré
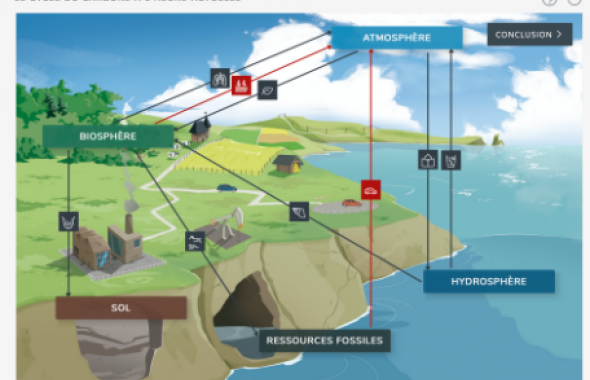
Etudie le cycle naturel du carbone en le construisant petit à petit puis visualise l'impact des activités humaines sur ce même cycle. Il est également possible de visualiser l'évolution de la concentration de dioxyde de carbone dans l'atmosphère.
Animation réalisée par l'OCE (Office for Climate Education - www.oce.global)
Découvrez L@map, la plateforme de formation en ligne pour les professeurs du premier degré et du collège.









